Page 15 - Himi - 1217
P. 15
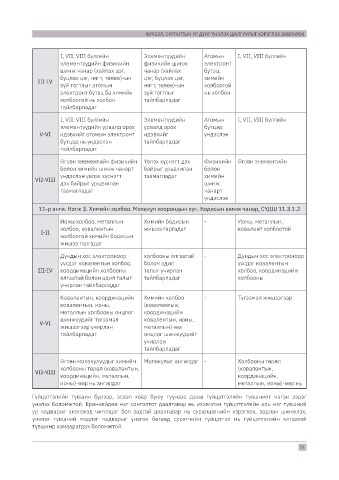
ХИЧЭЭЛ, СУРГАЛТЫН ҮР ДҮНГ ҮНЭЛЭХ ШАЛГУУРЫГ ХЭРЭГЛЭХ ЗӨВЛӨМЖ
I, VII, VIII бүлгийн Элементүүдийн Атомын I, VII, VIII бүлгийн
элементүүдийн физикийн физикийн шинж электронт
шинж чанар (хайлах цэг, чанар (хайлах бүтэц,
буцлах цэг, нягт, төлөв)-ын цэг, буцлах цэг, химийн
III-IV
зүй тогтлыг атомын нягт, төлөв)-ын холбоотой
электронт бүтэц ба химийн зүй тогтлыг нь холбон
холбоотой нь холбон тайлбарладаг
тайлбарладаг
I, VII, VIII бүлгийн Элементүүдийн Атомын I, VII, VIII бүлгийн
элементүүдийн урвалд орох урвалд орох бүтцэд
V-VI идэвхийг атомын электронт идэвхийг үндэслэн
бүтцэд нь үндэслэн тайлбарладаг
тайлбарладаг
Өгсөн элементийн физикийн Үелэх хүснэгт дэх Физикийн Өгсөн элементийн
болон химийн шинж чанарт байрыг урьдчилан болон
үндэслэн үелэх хүснэгт таамагладаг химийн
VII-VIII
дэх байрыг урьдчилан шинж
таамагладаг чанарт
үндэслэн
11-р анги. Нэгж 3. Химийн холбоо. Молекул хоорондын хүч. Бодисын шинж чанар, СҮДШ 11.3.1.2
Ионы холбоо, металлын Химийн бодисын - Ионы, металлын,
холбоо, ковалентын жишээ гаргадаг ковалент холбоотой
I-II
холбоотой химийн бодисын
жишээ гаргадаг
Дундын хос электроноор холбооны ялгаатай - Дундын хос электроноор
үүсдэг ковалентын холбоо, болон адил үүсдэг ковалентын
III-IV координацийн холбооны талыг учирлан холбоо, координацийн
ялгаатай болон адил талыг тайлбарладаг холбооны
учирлан тайлбарладаг
Ковалентын, координацийн Химийн холбоо - Түгээмэл жишээгээр
ковалентын, ионы, (ковалентын,
металлын холбооны онцлог координацийн
шинжүүдийг түгээмэл ковалентын, ионы,
V-VI
жишээгээр учирлан металлын)-ны
тайлбарладаг онцлог шинжүүдийг
учирлан
тайлбарладаг
Өгсөн молекулуудыг химийн Молекулыг ангилдаг - Холбооны төрөл
холбооны төрөл (ковалентын, (ковалентын,
VII-VIII
координацийн, металлын, координацийн,
ионы)-өөр нь ангилдаг металлын, ионы)-өөр нь
Гүйцэтгэлийн түвшин бүрээр, эсвэл хоёр буюу түүнээс дээш гүйцэтгэлийн түвшнийг нэгэн зэрэг
үнэлэх боломжтой. Ерөнхийдөө нэг сонголтот даалгавар нь ихэвчлэн гүйцэтгэлийн аль нэг түвшний
ур чадварыг үнэлэхэд чиглэдэг бол задгай даалгавар нь суралцагчийн хэрэглэх, задлан шинжлэх,
үнэлэх түвшний мэдлэг чадварыг үнэлэх бөгөөд сурагчийн гүйцэтгэл нь гүйцэтгэлийн ялгаатай
түвшинд хамаарагдах боломжтой.
11