Page 105 - Хими
P. 105
ХИЧЭЭЛ, СУРГАЛТЫН ҮР ДҮНГ ҮНЭЛЭХ ШАЛГУУР
Ижил энергитэй
р орбиталын орон
s, p атомын s, p атомын зайн ялгаатай p, d атомын
орбиталын орбиталын байрлалтай холбон орбиталаар
харьцангуй хэлбэрийг ижил энергитэй p , электрон
энергийн ялгааг тодорхойлдог p , p орбиталыг x хуваарилагдах
тодорхойлдог y z зүй тогтлыг
тодорхойлдог
тодорхойлдог
Элементийн
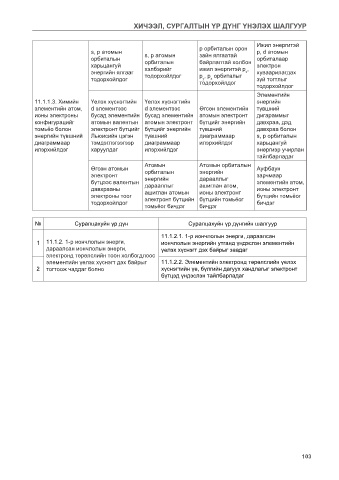
11.1.1.3. Химийн Үелэх хүснэгтийн Үелэх хүснэгтийн энергийн
элементийн атом, d элементээс d элементээс Өгсөн элементийн түвшний
ионы электроны бусад элементийн бусад элементийн атомын электронт дигараммыг
конфигурацийг атомын валентын атомын электронт бүтцийг энергийн давхраа, дэд
томьёо болон электронт бүтцийг бүтцийг энергийн түвшний давхраа болон
энергийн түвшний Льюисийн цэгэн түвшний диаграммаар s, p орбиталын
диаграммаар тэмдэглэгээгээр диаграммаар илэрхийлдэг харьцангуй
илэрхийлдэг харуулдаг илэрхийлдэг энергиэр учирлан
тайлбарладаг
Атомын Атомын орбиталын
Өгсөн атомын орбиталын энергийн Ауфбаун
электронт энергийн дарааллыг зарчмаар
бүтцээс валентын дарааллыг ашиглан атом, элементийн атом,
давхрааны ашиглан атомын ионы электронт ионы электронт
электроны тоог электронт бүтцийн бүтцийн томьёог бүтцийн томьёог
тодорхойлдог бичдэг
томьёог бичдэг бичдэг
№ Суралцахуйн үр дүн Суралцахуйн үр дүнгийн шалгуур
11.1.2.1. 1-р иончлолын энерги, дараалсан
1 11.1.2. 1-р иончлолын энерги, иончлолын энергийн утганд үндэслэн элементийн
дараалсан иончлолын энерги, үелэх хүснэгт дэх байрыг заадаг
электронд төрөлслийн тоон холбогдлоос
элементийн үелэх хүснэгт дэх байрыг 11.1.2.2. Элементийн электронд төрөлслийн үелэх
2 тогтоож чаддаг болно хүснэгтийн үе, бүлгийн дагуух хандлагыг электронт
бүтцэд үндэслэн тайлбарладаг
103